公司新闻
香港 2018年8月22日
亿胜生物科技有限公司(“亿胜生物”或“集团”;股份代号:1061)欣然公布,集团间接全资附属公司珠海亿胜生物制药有限公司已获国家药品监督管理局批准于中华人民共和国进行不含防腐剂玻璃酸钠单剂量滴眼液注册及商业化。该个获批产品已经是集团第三个获得国家药品监督管理局(「药监局」)批准上市的不含防腐剂单剂量滴眼液。另外两个不含防腐剂单剂量滴眼液,妥布霉素以及左氧氟沙星,已分别于2017年4月(2018年3月获得GMP认证)及2018年6月获得药监局批准上市。
集团预计上述三个不含防腐剂单剂量滴眼液将于2018年第四季度在市场上正式销售。董事会相信上述获批产品将进一步充实集团眼科产品组合,从而增强集团在眼科之市场地位。
关于玻璃酸钠滴眼液
玻璃酸钠滴眼液目前广泛用于治疗干燥综合症(Sjögren’s Syndrome)﹑斯· 约二氏综合症(Stevens-Johnson Syndrome) ﹑干眼综合症(Dry Eye Syndrome)等内因性疾患;手术后﹑药物性﹑外伤、配戴隐形眼镜等外因性疾患。此外,玻璃酸钠滴眼液也获列入2017年全国医保目录。据米内网最新数据显示,国内玻璃酸钠滴眼液整体销售额近年稳步提升,近三年年均复合增长率接近20%,为前五大眼科用药之一。
关于“吹-灌-封”单剂量平台
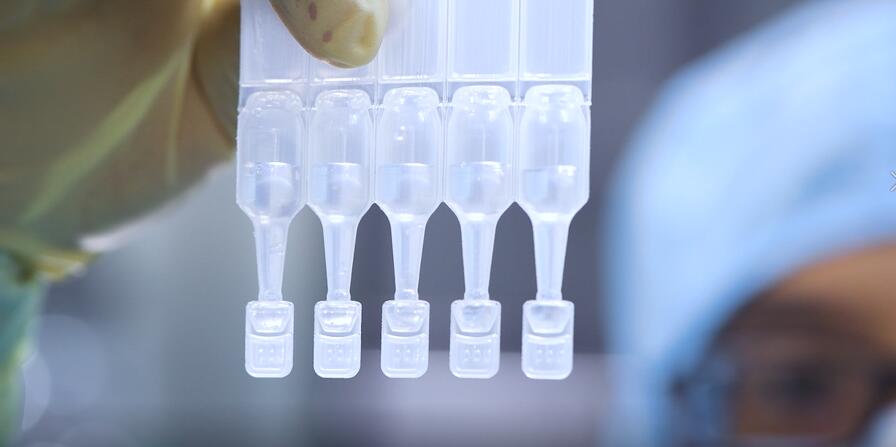
作为集团核心研发平台之一,亿胜“吹-灌-封”单剂量平台为先进的生产制造平台,用作开发及生产一系列无防腐剂单剂量药品,尤其是眼科药物。除了已获上市批准的不含防腐剂妥布霉素、左氧氟沙星以及玻璃酸钠单剂量滴眼液,目前集团仍有7种该等产品处于研发当中,分别用于治疗眼部损伤、眼部细菌感染、眼睛疲劳、干眼症及呼吸系统疾病,预期将于未来三年内陆续获得药监局商业化批准。
亿胜生物科技有限公司(“亿胜生物”或“集团”;股份代号:1061)欣然公布,集团间接全资附属公司珠海亿胜生物制药有限公司已获国家药品监督管理局批准于中华人民共和国进行不含防腐剂玻璃酸钠单剂量滴眼液注册及商业化。该个获批产品已经是集团第三个获得国家药品监督管理局(「药监局」)批准上市的不含防腐剂单剂量滴眼液。另外两个不含防腐剂单剂量滴眼液,妥布霉素以及左氧氟沙星,已分别于2017年4月(2018年3月获得GMP认证)及2018年6月获得药监局批准上市。
集团预计上述三个不含防腐剂单剂量滴眼液将于2018年第四季度在市场上正式销售。董事会相信上述获批产品将进一步充实集团眼科产品组合,从而增强集团在眼科之市场地位。
关于玻璃酸钠滴眼液
玻璃酸钠滴眼液目前广泛用于治疗干燥综合症(Sjögren’s Syndrome)﹑斯· 约二氏综合症(Stevens-Johnson Syndrome) ﹑干眼综合症(Dry Eye Syndrome)等内因性疾患;手术后﹑药物性﹑外伤、配戴隐形眼镜等外因性疾患。此外,玻璃酸钠滴眼液也获列入2017年全国医保目录。据米内网最新数据显示,国内玻璃酸钠滴眼液整体销售额近年稳步提升,近三年年均复合增长率接近20%,为前五大眼科用药之一。
关于“吹-灌-封”单剂量平台
作为集团核心研发平台之一,亿胜“吹-灌-封”单剂量平台为先进的生产制造平台,用作开发及生产一系列无防腐剂单剂量药品,尤其是眼科药物。除了已获上市批准的不含防腐剂妥布霉素、左氧氟沙星以及玻璃酸钠单剂量滴眼液,目前集团仍有7种该等产品处于研发当中,分别用于治疗眼部损伤、眼部细菌感染、眼睛疲劳、干眼症及呼吸系统疾病,预期将于未来三年内陆续获得药监局商业化批准。
相关新闻


































































 粤公网安备 44049102496184号
粤公网安备 44049102496184号