傳媒聚焦
Imoney智富雜誌:多項產品進入衝刺階段 億勝生物放眼未來十年
2021.03.22
億勝生物科技( 01061.HK )現在銷售網絡已覆蓋中國近9,000間醫院,同時已衝出海外,未來產品研發若取得突破,將令收入提高至另一台階。
億勝生物科技去年收入按年跌23.6%至9.8億元,主要由於去年上半年疫情的防控措施,影響醫院日常運作,公司產品主打眼科及外科創傷修復,相關非緊急病人無法就診,因此去年上半年業務受到較大影響。公司在去年第三季已逐步回返正軌,下半年收入按年僅跌6.2%(見圖一)。疫情影響僅屬短暫,億勝生物科技在2001年上市,主席嚴名熾認為公司要持續發展,一方面需要強化及開拓產品線,另一方面企業要年輕化,實際上嚴名熾的兒子嚴賢龍亦於2015年已加入公司,開始接手公司的未來發展。
新產品帶來二十年收入
嚴名熾補充指:「我們之前訂立2016年到2025年的10年計劃,稱之為增值計劃(Enrichment Program),目標是在2025年有多種在全球達到創新及領先水平的產品。」他介紹指,有4個產品線已進入三期臨床階段,預計在現有9項產品的產品線上,2025年或之前投入到市場。
「當我們發展一個好的產品線,就足以支持我們的收入近20年。例如貝復舒系列於1998年開始推出,至今仍是我們的主要產品之一。」談及公司下一步的發展,嚴名熾分析指:「中國政府規定手術後的藥品不得含有防腐劑,正是我們眼科產品的優勢。我們的貝復舒進入了《2020年中國乾眼專家共識》,未來將加強術後修復及乾眼症的領域。」
着手部署新10年計劃
由公司附屬與Mitotech共同開發、用於乾眼症含SkQ1的滴眼液,上月在美國臨床獲得正面結果。中央角膜熒光素染色數據及最佳矯正視力改善都報喜,研究亦突出該葯安全性,耐受性與人工淚液相似。公司指對第三階段三期臨床試驗結果充滿期待,目標於2022年至2023完成提交NDA。
嚴名熾強調SkQ1不具刺激性,而美國在乾眼症的市場達到近62億美元,若產品順利於2023年面世,將於未來20年帶動公司收入增長。他強調該產品將是全球第一及唯一。
他又透露,公司已訂立新的10年計劃,預期將推出1至3個重磅產品,其中包括針對抗藥性的藥物:「現時市面一些藥物因為抗藥性,用了兩年就失去作用,我們正在對此作出研發工作。」
產品於國際並不遜色
醫藥行業離不開政策的影響,嚴名熾認為中國政府一直支持創新葯:「醫藥管理局的政策一直配合創新葯的發展,鼓勵葯企進行創新及改善質素。億勝一直以創新葯為主,反而一些過去以仿製葯為主的葯企,要轉向創新葯並非容易。」
嚴名熾又表示,億勝旗下不少創新葯已被納入醫保名單,而公司並不只放眼本地市場,更希望在國際市場都做到創新:「例如公司的再生因子產品是全球唯一,而其他產品如乾眼症藥物SkQ1亦要做到在全球層面創新及最佳( First in Class and Best in Class )。」現在公司再生因子產品在中國眼科市佔率達到近六成,外科創傷修復佔四成。
高研發開支投資未來
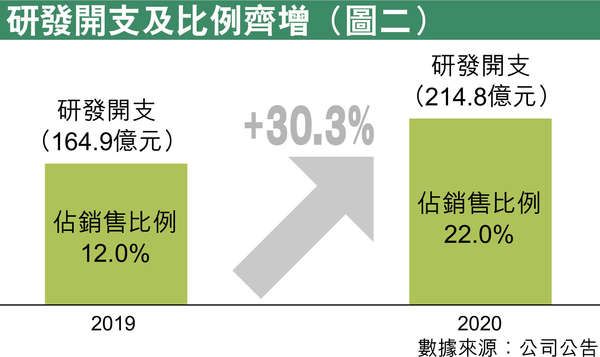
公司以創新葯為主,研發中心位於中國、英國、美國及新加坡,現在公司研發開支占銷售佔比維持近兩成的水平(見圖二)。嚴名熾解釋:「一來多項產品進入三期臨床,甚至部分進入全球臨床試驗。一般進行全球臨床試驗,研發開支將達到2,000至4,000萬美元。」不過,他認為最終這些投資都會轉化為產品在全球銷售。
「強化產品線、加強國際銷售渠道、適應政策,是我們的目標。」嚴表示,除了內部研發外,公司一直有考慮併購及授權經營。他認為併購不只看產品本身,而是能否延伸到其他地方,成為一系列的產品,不浪費公司的投入。
問及有沒有意願回A股或分拆項目上市,嚴名熾指回A股同時保留香港上市平台,要處理很多安排,強調公司管理層將優先專註於業務發展。公司現在擴產,產能由每小時9,000劑增加至33,000劑,涉及資本開支約4,000萬元人民幣,來源以自有資金為主,並沒有短期融資計劃。嚴名熾最後總結指:「中小型上市公司一般的問題是透明度及業務持續性不高,而我們目標是與大型的上市公司一樣,通過業務增長持續為投資者財富增值。」
眼科產品重視安全性
根據Frost&Sullivan,中國眼科用藥在2019年到2030年複合平均增長率達到17.8%,未來增長前景甚佳。眼科產品涉及的專業知識眾多,嚴名熾認為眼疾大致可分為幾類,包括眼角膜、晶體、眼底及眼壓。其中最重要及最常見是眼角膜,如手術或其他原因引起的乾眼症。晶體最常見毛病是白內障、眼壓最常見的異常是青光眼。另外,眼底主要指視網膜,除了老年退化問題外,黃斑病等都需要更有效的藥物。 嚴名熾強調眼晴比較敏感,安全性非常重要,例如公司玻璃酸眼滴液產品不含防腐劑,以免令病人出現過敏。
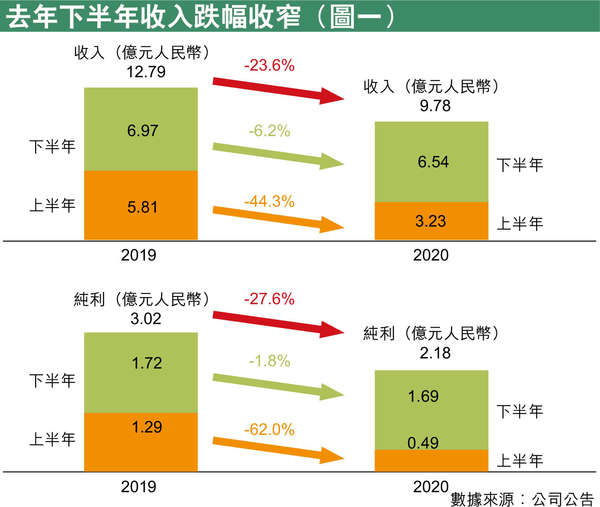
億勝生物科技去年收入按年跌23.6%至9.8億元,主要由於去年上半年疫情的防控措施,影響醫院日常運作,公司產品主打眼科及外科創傷修復,相關非緊急病人無法就診,因此去年上半年業務受到較大影響。公司在去年第三季已逐步回返正軌,下半年收入按年僅跌6.2%(見圖一)。疫情影響僅屬短暫,億勝生物科技在2001年上市,主席嚴名熾認為公司要持續發展,一方面需要強化及開拓產品線,另一方面企業要年輕化,實際上嚴名熾的兒子嚴賢龍亦於2015年已加入公司,開始接手公司的未來發展。
新產品帶來二十年收入
嚴名熾補充指:「我們之前訂立2016年到2025年的10年計劃,稱之為增值計劃(Enrichment Program),目標是在2025年有多種在全球達到創新及領先水平的產品。」他介紹指,有4個產品線已進入三期臨床階段,預計在現有9項產品的產品線上,2025年或之前投入到市場。
「當我們發展一個好的產品線,就足以支持我們的收入近20年。例如貝復舒系列於1998年開始推出,至今仍是我們的主要產品之一。」談及公司下一步的發展,嚴名熾分析指:「中國政府規定手術後的藥品不得含有防腐劑,正是我們眼科產品的優勢。我們的貝復舒進入了《2020年中國乾眼專家共識》,未來將加強術後修復及乾眼症的領域。」
着手部署新10年計劃
由公司附屬與Mitotech共同開發、用於乾眼症含SkQ1的滴眼液,上月在美國臨床獲得正面結果。中央角膜熒光素染色數據及最佳矯正視力改善都報喜,研究亦突出該葯安全性,耐受性與人工淚液相似。公司指對第三階段三期臨床試驗結果充滿期待,目標於2022年至2023完成提交NDA。
嚴名熾強調SkQ1不具刺激性,而美國在乾眼症的市場達到近62億美元,若產品順利於2023年面世,將於未來20年帶動公司收入增長。他強調該產品將是全球第一及唯一。
他又透露,公司已訂立新的10年計劃,預期將推出1至3個重磅產品,其中包括針對抗藥性的藥物:「現時市面一些藥物因為抗藥性,用了兩年就失去作用,我們正在對此作出研發工作。」
產品於國際並不遜色
醫藥行業離不開政策的影響,嚴名熾認為中國政府一直支持創新葯:「醫藥管理局的政策一直配合創新葯的發展,鼓勵葯企進行創新及改善質素。億勝一直以創新葯為主,反而一些過去以仿製葯為主的葯企,要轉向創新葯並非容易。」
嚴名熾又表示,億勝旗下不少創新葯已被納入醫保名單,而公司並不只放眼本地市場,更希望在國際市場都做到創新:「例如公司的再生因子產品是全球唯一,而其他產品如乾眼症藥物SkQ1亦要做到在全球層面創新及最佳( First in Class and Best in Class )。」現在公司再生因子產品在中國眼科市佔率達到近六成,外科創傷修復佔四成。
高研發開支投資未來
公司以創新葯為主,研發中心位於中國、英國、美國及新加坡,現在公司研發開支占銷售佔比維持近兩成的水平(見圖二)。嚴名熾解釋:「一來多項產品進入三期臨床,甚至部分進入全球臨床試驗。一般進行全球臨床試驗,研發開支將達到2,000至4,000萬美元。」不過,他認為最終這些投資都會轉化為產品在全球銷售。
「強化產品線、加強國際銷售渠道、適應政策,是我們的目標。」嚴表示,除了內部研發外,公司一直有考慮併購及授權經營。他認為併購不只看產品本身,而是能否延伸到其他地方,成為一系列的產品,不浪費公司的投入。
問及有沒有意願回A股或分拆項目上市,嚴名熾指回A股同時保留香港上市平台,要處理很多安排,強調公司管理層將優先專註於業務發展。公司現在擴產,產能由每小時9,000劑增加至33,000劑,涉及資本開支約4,000萬元人民幣,來源以自有資金為主,並沒有短期融資計劃。嚴名熾最後總結指:「中小型上市公司一般的問題是透明度及業務持續性不高,而我們目標是與大型的上市公司一樣,通過業務增長持續為投資者財富增值。」
眼科產品重視安全性
根據Frost&Sullivan,中國眼科用藥在2019年到2030年複合平均增長率達到17.8%,未來增長前景甚佳。眼科產品涉及的專業知識眾多,嚴名熾認為眼疾大致可分為幾類,包括眼角膜、晶體、眼底及眼壓。其中最重要及最常見是眼角膜,如手術或其他原因引起的乾眼症。晶體最常見毛病是白內障、眼壓最常見的異常是青光眼。另外,眼底主要指視網膜,除了老年退化問題外,黃斑病等都需要更有效的藥物。 嚴名熾強調眼晴比較敏感,安全性非常重要,例如公司玻璃酸眼滴液產品不含防腐劑,以免令病人出現過敏。










 粤公网安备 44049102496184号
粤公网安备 44049102496184号